Атомы — мельчайшие частицы вещества.
Если увеличить до размеров Земного шара яблоко средней величины, то атомы станут размером всего лишь с яблоко. Несмотря на столь малые размеры, атом состоит из еще более мелких физических частиц.
Со строением атома вы должны быть уже знакомы из школьного курса физики. И все-таки напомним, что в составе атома есть ядро и электроны, которые вращаются вокруг ядра так быстро, что становятся неразличимыми — образуют «электронное облако», или электронную оболочку атома.
Электроны принято обозначать так: e − . Электроны e − очень легкие, почти невесомые, но зато имеют отрицательный электрический заряд. Он равен −1. Электрический ток, которым все мы пользуемся — это поток электронов, бегущий в проводах.
Ядро атома, в котором сосредоточена почти вся его масса, состоит из частиц двух сортов — нейтронов и протонов.
Нейтроны обозначают так: n 0 , а протоны так: p + .
По массе нейтроны и протоны почти одинаковы — 1,675 · 10 −24 г и 1,673 · 10 −24 г.
Правда, считать массу таких маленьких частиц в граммах очень неудобно, поэтому ее выражают в углеродных единицах, каждая из которых равна 1,673 · 10 −24 г.
Для каждой частицы получают относительную атомную массу, равную частному от деления массы атома (в граммах) на массу углеродной единицы. Относительные атомные массы протона и нейтрона равны 1, а вот заряд у протонов положительный и равен +1, в то время как у нейтронов заряда нет.
- Первое условие: каждому виду атомов соответствует свой собственный набор «деталей» — элементарных частиц. Например, в атоме водорода обязательно будет ядро с положительным зарядом +1, значит, в нем непременно должен быть один протон (и не больше).
В атоме водорода могут быть и нейтроны. Об этом — в следующем параграфе.
Атом кислорода (порядковый номер в Периодической системе равен 8) будет иметь ядро, заряженное восемью положительными зарядами (+8), — значит, там восемь протонов. Поскольку масса атома кислорода равна 16 относительных единиц, чтобы получить ядро кислорода, добавим еще 8 нейтронов. - Второе условие состоит в том, чтобы каждый атом оказался электронейтральным. Для этого в нем должно быть электронов столько, чтобы уравновесить заряд ядра. Иначе говоря, число электронов в атоме равно числу протонов в его ядре, а также порядковому номеру этого элемента в Периодической системе.
Задание 10 . Определите состав атомов
При ответе рекомендуется использовать Таблицу Менделеева.
Из чего все состоит
Величина заряда дана в кулонах, масса — в килограммах (единицах СИ); слова «спин» и «статистика» будут пояснены ниже.
Обратим внимание на различие в массе частиц: протоны и нейтроны почти в 2000 раз тяжелее электронов. Следовательно, масса любого тела почти целиком определяется массой протонов и нейтронов.
Лучшая модель атома? [Минутка физики]
Нейтрон, как это следует из его названия, нейтрален — его заряд равен нулю. А протон и электрон имеют одинаковые по величине, но противоположные по знаку заряды. Электрон заряжен отрицательно, а протон — положительно.
Среди характеристик частиц нет, казалось бы, важной характеристики — их размера. Описывая строение атомов и молекул, электроны, протоны и нейтроны можно считать материальными точками. О размерах протона и нейтрона придется вспомнить только при описании атомных ядер. Даже по сравнению с размерами атомов протоны и нейтроны чудовищно малы (порядка 10 -16 метра).
По сути дела, этот короткий раздел сводится к представлению электронов, протонов и нейтронов как строительного материала всех тел в природе. Можно было бы просто ограничиться таблицей 1, однако нам предстоит понять, каким образом из электронов, протонов и нейтроновосуществляется постройка, что заставляет частицы объединяться в более сложные конструкции и каковы эти конструкции .
АТОМ — НАИБОЛЕЕ ПРОСТАЯ ИЗ СЛОЖНЫХ КОНСТРУКЦИЙ
Атомов много. Оказалось необходимым и возможным упорядочить их специальным образом. Упорядочение дает возможность подчеркнуть различие и сходство атомов. Разумное расположение атомов — заслуга Д. И. Менделеева (1834-1907), который сформулировал периодический закон, носящий его имя. Если временно отвлечься от существования периодов, то принцип расположения элементов крайне прост: они располагаются последовательно по весу атомов. Самый легкий — атом водорода. Последний природный (не созданный искусственно) атом — атом урана, который тяжелее его в 200 с лишним раз.
Понимание строения атомов объяснило наличие периодичности в свойствах элементов.
В самом начале XX века Э. Резерфорд (1871-1937) убедительно показал, что почти вся масса атома сосредоточена в его ядре — небольшой (даже по сравнению с атомом) области пространства: радиус ядра приблизительно в 100 тысяч раз меньше размера атома. Когда Резерфорд производил свои эксперименты, еще не был открыт нейтрон. С открытием нейтрона было понято, что ядра состоят из протонов и нейтронов, а атом естественно представлять себе как ядро, окруженное электронами, число которых равно числу протонов в ядре — ведь в целом атом нейтрален. Протоны и нейтроны, как строительныйматериал ядра, получили общее название — нуклоны(с латинского nucleus — ядро). Этим названием мы и будем пользоваться.
Количество нуклонов в ядре принято обозначать буквой А. Ясно, что А = N + Z, где N — число нейтронов в ядре, а Z — число протонов, равное числу электронов в атоме. Число А носит название атомной массы, а Z — атомного номера. Атомы с одинаковыми атомными номерами называют изотопами: в таблице Менделеева они находятся в одной клеточке (по-гречески изос — равный, топос — место). Дело в том, что химические свойства изотопов почти тождественны. Если таблицу Менделеева рассмотреть внимательно, можно убедиться, что, строго говоря, расположение элементов соответствует не атомной массе, а атомному номеру. Если элементов около 100, то изотопов более 2000. Правда, многие из них неустойчивы, то есть радиоактивны (от латинского radio — излучаю, activus — деятельный), они распадаются, испуская различные излучения.
Опыты Резерфорда не только привели к открытию атомных ядер, но и показали, что в атоме действуют те же электростатические силы, которые отталкивают друг от друга одноименно заряженные тела и притягивают друг к другу разноименно заряженные (например, шарики электроскопа).
Атом устойчив. Следовательно, электроны в атоме движутся вокруг ядра: центробежная сила компенсирует силу притяжения. Понимание этого привело к созданию планетарной модели атома, в которой ядро — Солнце, а электроны — планеты (с точки зрения классической физики, планетарная модель непоследовательна, но об этом ниже).
Есть целый ряд способов оценить размер атома. Разные оценки приводят к близким результатам: размеры атомов, конечно, различны, но приблизительно равны нескольким десятым нанометра (1 нм = 10 -9 м).
Рассмотрим для начала систему электронов атома.
В Солнечной системе планеты притягиваются к Солнцу силой гравитации. В атоме действует электростатическая сила. Ее часто называют кулоновской в честь Шарля Огюстена Кулона (1736-1806), установившего, что сила взаимодействия между двумя зарядами обратно пропорциональна квадрату расстояния между ними. Тот факт, что два заряда Q1 и Q2 притягиваются или отталкивают ся с силой, равной FC = Q1Q2/r 2 , где r — расстояние между зарядами, носит название «Закон Кулона». Индекс «С» присвоен силе F по первой букве фамилии Кулона (по-французски Coulomb ). Среди самых различных утверждений мало найдется таких, которые столь же справедливо названы законом, как закон Кулона: ведь область его применимости практически не ограничена. Заряженные тела, каких бы они ни были размеров, а также атомные и даже субатомные заряженные частицы — все они притягиваются или отталкиваются в согласии с законом К
Fatal error: Uncaught Error: Call to undefined function set_magic_quotes_runtime() in /www/htdocs/1dbcf2b3552b065fc49d8747114db86c/sape.php:262 Stack trace: #0 /www/htdocs/1dbcf2b3552b065fc49d8747114db86c/sape.php(343): SAPE_base->_read(‘/www/htdocs/1db. ‘) #1 /www/htdocs/1dbcf2b3552b065fc49d8747114db86c/sape.php(418): SAPE_base->load_data() #2 /www/htdocs/links.html(7): SAPE_client->SAPE_client() #3 /www/htdocs/happy_physics/kaganov4.html(128): include(‘/www/htdocs/lin. ‘) #4 thrown in /www/htdocs/1dbcf2b3552b065fc49d8747114db86c/sape.php on line 262
Атом
Атом — это наименьшая частица химического элемента, сохраняющая все его химические свойства. Атом состоит из ядра, имеющего положительный электрический заряд, и отрицательно заряженных электронов. Заряд ядра любого химического элемента равен произведению Z на e, где Z — порядковый номер данного элемента в периодической системе химических элементов, е — величина элементарного электрического заряда.
Электрон — это мельчайшая частица вещества с отрицательным электрическим зарядом е=1,6·10 -19 кулона, принятым за элементарный электрический заряд. Электроны, вращаясь вокруг ядра, располагаются на электронных оболочках К, L, М и т. д. К — оболочка, ближайшая к ядру. Размер атома определяется размером его электронной оболочки. Атом может терять электроны и становиться положительным ионом или присоединять электроны и становиться отрицательным ионом. Заряд иона определяет число потерянных или присоединенных электронов. Процесс превращения нейтрального атома в заряженный ион называется ионизацией.
Атомное ядро (центральная часть атома) состоит из элементарных ядерных частиц — протонов и нейтронов. Радиус ядра примерно в сто тысяч раз меньше радиуса атома. Плотность атомного ядра чрезвычайно велика. Протоны — это стабильные элементарные частицы, имеющие единичный положительный электрический заряд и массу, в 1836 раз большую, чем масса электрона. Протон представляет собой ядро атома самого легкого элемента — водорода. Число протонов в ядре равно Z. Нейтрон — это нейтральная (не имеющая электрического заряда) элементарная частица с массой, очень близкой к массе протона. Поскольку масса ядра складывается из массы протонов и нейтронов, то число нейтронов в ядре атома равно А — Z, где А — массовое число данного изотопа (см. Периодическая система химических элементов). Протон и нейтрон, входящие в состав ядра, называются нуклонами. В ядре нуклоны связаны особыми ядерными силами.
В атомном ядре имеется огромный запас энергии, которая высвобождается при ядерных реакциях. Ядерные реакции возникают при взаимодействии атомных ядер с элементарными частицами или с ядрами других элементов. В результате ядерных реакций образуются новые ядра. Например, нейтрон может переходить в протон. В этом случае из ядра выбрасывается бета-частица, т. е. электрон.
Переход в ядре протона в нейтрон может осуществляться двумя путями: либо из ядра испускается частица с массой, равной массе электрона, но с положительным зарядом, называемая позитроном (позитронный распад), либо ядро захватывает один из электронов с ближайшей к нему К-оболочки (К-захват).
Иногда образовавшееся ядро обладает избытком энергии (находится в возбужденном состоянии) и, переходя в нормальное состояние, выделяет лишнюю энергию в виде электромагнитного излучения с очень малой длиной волны — гамма-излучение. Энергия, выделяющаяся при ядерных реакциях, практически используется в различных отраслях промышленности.


Атом (греч. atomos — неделимый) наименьшая частица химического элемента, обладающая его химическими свойствами. Каждый элемент состоит из атомов определенного вида. В состав атома входят ядро, несущее положительный электрический заряд, и отрицательно заряженные электроны (см.), образующие его электронные оболочки. Величина электрического заряда ядра равна Z-e, где е — элементарный электрический заряд, равный по величине заряду электрона (4,8·10 —10 эл.-ст. ед.), и Z — атомный номер данного элемента в периодической системе химических элементов (см.). Так как неионизированный атом нейтрален, то число электронов, входящих в него, также равно Z. В состав ядра (см. Ядро атомное) входят нуклоны, элементарные частицы с массой, примерно в 1840 раз большей массы электрона (равной 9,1·10 -28 г), протоны (см.), заряженные положительно, и не имеющие заряда нейтроны (см.). Число нуклонов в ядре называется массовым числом и обозначается буквой А. Количество протонов в ядре, равное Z, определяет число входящих в атом электронов, строение электронных оболочек и химические свойства атома. Количество нейтронов в ядре равно А—Z. Изотопами называются разновидности одного и того же элемента, атомы которых отличаются друг от друга массовым числом А, но имеют одинаковые Z. Таким образом, в ядрах атомов различных изотопов одного элемента имеется разное число нейтронов при одинаковом числе протонов. При обозначении изотопов массовое число А записывается сверху от символа элемента, а атомный номер внизу; например, изотопы кислорода обозначаются:
Размеры атома определяются размерами электронных оболочек и составляют для всех Z величину порядка 10 —8 см. Поскольку масса всех электронов атома в несколько тысяч раз меньше массы ядра, масса атома пропорциональна массовому числу. Относительная масса атома данного изотопа определяется по отношению к массе атома изотопа углерода С 12 , принятой за 12 единиц, и называется изотопной массой. Она оказывается близкой к массовому числу соответствующего изотопа. Относительный вес атома химического элемента представляет собой среднее (с учетом относительной распространенности изотопов данного элемента) значение изотопного веса и называется атомным весом (массой).
Атом является микроскопической системой, и его строение и свойства могут быть объяснены лишь при помощи квантовой теории, созданной в основном в 20-е годы 20 века и предназначенной для описания явлений атомного масштаба. Опыты показали, что микрочастицы — электроны, протоны, атомы и т. д.,— кроме корпускулярных, обладают волновыми свойствами, проявляющимися в дифракции и интерференции. В квантовой теории для описания состояния микрообъектов используется некоторое волновое поле, характеризуемое волновой функцией (Ψ-функция). Эта функция определяет вероятности возможных состояний микрообъекта, т. е. характеризует потенциальные возможности проявления тех или иных его свойств. Закон изменения функции Ψ в пространстве и времени (уравнение Шредингера), позволяющий найти эту функцию, играет в квантовой теории ту же роль, что в классической механике законы движения Ньютона. Решение уравнения Шредингера во многих случаях приводит к дискретным возможным состояниям системы. Так, например, в случае атома получается ряд волновых функций для электронов, соответствующих различным (квантованным) значениям энергии. Система энергетических уровней атома, рассчитанная методами квантовой теории, получила блестящее подтверждение в спектроскопии. Переход атома из основного состояния, соответствующего низшему энергетическому уровню Е0, в какое-либо из возбужденных состояний Ei происходит при поглощении определенной порции энергии Еi — Е0. Возбужденный атом переходит в менее возбужденное или основное состояние обычно с испусканием фотона. При этом энергия фотона hv равна разности энергий атома в двух состояниях: hv= Ei— Еk где h — постоянная Планка (6,62·10 —27 эрг·сек), v — частота света.
Кроме атомных спектров, квантовая теория позволила объяснить и другие свойства атомов. В частности, были объяснены валентность, природа химической связи и строение молекул, создана теория периодической системы элементов.
- Анатомический атлас
- Физиология человека
- Детские болезни
- Йога
- Правильное питание
- Как похудеть
- ЛФК (лечебная физкультура)
- Лучшие курорты мира
- Лечение народными средствами
- Лекарственные растения
- Проктология
- Психиатрия
- Алкоголизм
- Курение
- Спортивная медицина
- Судебная медицина
Атомы
На сегодняшний день известно (118) видов атомов. Более (90) из них существуют в природе, а остальные получены искусственно.
Атомы характеризуются:
- определёнными очень малыми размерами;
- определённой, тоже очень малой, массой;
- определённым строением.
Размеры атомов настолько малы, что увидеть их невозможно даже в самый мощный микроскоп. Радиусы атомов составляют (0,046)–(0,25) нм ((1) нм (=) 10 − 9 м). Самый маленький — атом гелия, а самый большой — франция.
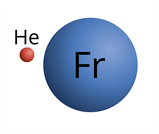
Рис. (1). Атомы гелия и франция
Массы атомов тоже ничтожно малы. Так масса атома водорода составляет всего 1,67 ⋅ 10 − 24 г.
До конца (19)-го столетия атомы считали неделимыми частицами. Но учёные доказали, что атом имеет сложное строение.
Согласно современным представлениям каждый атом состоит из положительно заряженного ядра и движущихся вокруг него электронов . Электроны имеют отрицательный заряд и нейтрализуют положительный заряд ядра.
Ядро намного меньше самого атома. Так, радиус атома водорода составляет (0,046) нм, а радиус его ядра — всего (0,00000065) нм. В его состав входят ещё более мелкие частицы: протоны ((p)) и нейтроны ((n)). Протоны заряжены положительно и определяют заряд ядра. Нейтроны — частицы без заряда.
Заряд протона равен по величине заряду электрона, а число протонов в ядре равно числу электронов в атоме. Поэтому атомы нейтральны.
Атомы различаются между собой строением (числом содержащихся в них частиц), а также массой и размерами.
Рис. (2). Атом гелия
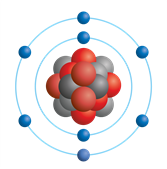
Рис. (3). Атом кислорода
В химических реакциях атомы не изменяются, а только перегруппировываются — объединяются в новых комбинациях.
Атом — мельчайшая химически неделимая электронейтральная частица вещества, состоящая из положительного ядра и отрицательных электронов.
Атомы не изменяются в химических реакциях, но существуют ядерные реакции, при протекании которых их строение изменяется.
Атомы редко встречаются в изолированном виде. Обычно они соединяются друг с другом в молекулы или более крупные структуры. Число вариантов соединения атомов практически бесконечно, и их относительно небольшое число приводит к образованию огромного количества разнообразных веществ.
Что говорит Дон Линкольн
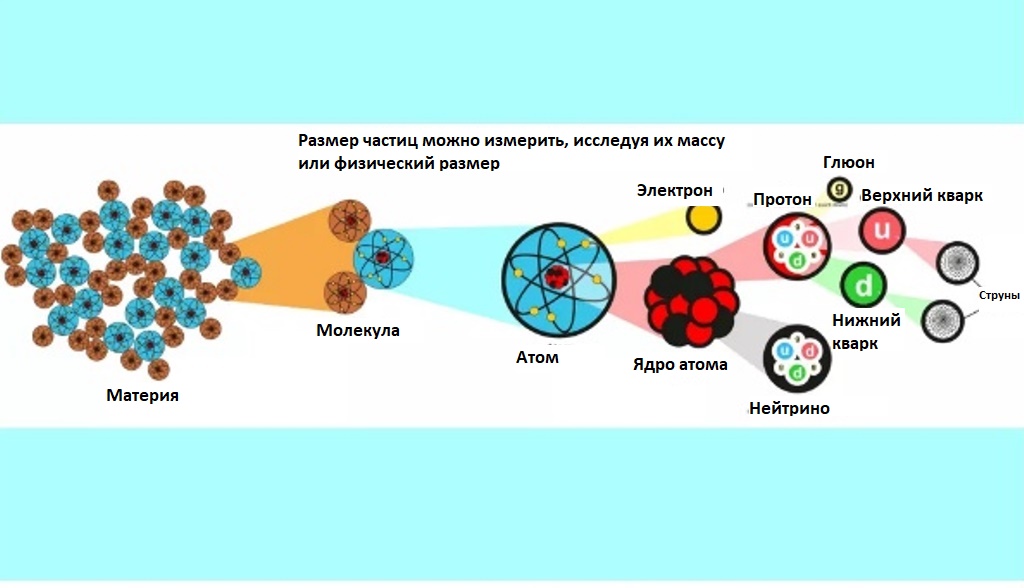
Дон Линкольн, сотрудник Национальной ускорительной лаборатории им. Ферми (Фермилаб), которая находится недалеко от Чикаго, является одним из исследователей, желающих понять, какая частица во Вселенной самая крохотная, а какая самая большая. В Фермилабе ученые применяют ускоритель, при помощи которого разбивают атомы и изучают их обломки. Линкольн говорит, что размер частиц можно замерить двумя способами:
- Определить их физический размер (к примеру, вычислить диаметр шара).
- Установить их массу.
Самая крохотная частица

С точки зрения массы на вышеуказанные вопросы легко дать ответ. Линкольн заявил, что из всех известных частиц лишь нейтрино имеет самую небольшую массу. Но он указал, что мы не можем точно измерить вес нейтрино, потому что приборы, применяемые для определения массы элементарных частиц, малочувствительны.
«Нейтрино представляет собой некий призрак субатомной вселенной», — сказал ученый. Известно, что нейтрино слабо контактирует с любым веществом и по численности является вторым после фотонов. Фактически именно в это мгновение через вас пролетают триллионы нейтрино. Эти частицы перемещаются со скоростью, почти идентичной скорости света.
Ядро любого атома состоит из электронов, нейтронов и протонов. Линкольн утверждает, что нейтроны и протоны составляют 1/10 размера ядра. Электрон имеет массу, которая близка к нулю, но в действительности весит в 500 000 раз больше, чем нейтрино. Из этого следует, что самая маленькая частица весит намного меньше электрона.
ЭЛЕМЕНТАРНЫЕ ЧАСТИЦЫ
Материя в природе присутствует в двух качественно различных формах: вещества и физических полей. Вещество состоит из молекул, молекулы построены из атомов, а атомы состоят из электронов и ядер. Ядра включают в себя протоны и нейтроны. Электроны, протоны и нейтроны называют элементарными частицами.
Что касается полей, то существует несколько их видов, в том числе электромагнитное и гравитационное. Посредством полей объекты могут взаимодействовать друг с другом, поля также обеспечивают передачу энергии от одних объектов к другим. В настоящее время твердо установлено, что электромагнитное поле также представляет собой совокупность элементарных частиц, называемых фотонами.
В данном разделе мы рассмотрим строение элементарных частиц с более детальным анализом тех свойств, которые потребуются нам при дальнейшем изучении основ физической химии.
СТРОЕНИЕ И СВОЙСТВА ЭЛЕМЕНТАРНЫХ ЧАСТИЦ
Элементарные частицы — это мельчайшие, первичные частицы вещества, которые нельзя разделить на свободные частицы других типов.
В настоящее время это определение перестало быть вполне строгим, и под термином «элементарные» теперь понимают большую группу мельчайших частиц, не являющихся ядрами или атомами. Число элементарных частиц достаточно велико — около 350. Структура элементарных частиц далеко не проста. Такие частицы, как протон и нейтрон, состоят из других частиц — кварков, которые в свободном состоянии не существуют. Не исключено, что частицы устроены по принципу «матрешки» — одна частица включает в себя другие частицы, другие включают третьи и т.д. Несмотря на то, что кварки важны для понимания структуры протонов и нейтронов, мы не будем вдаваться в эту сложную область физики элементарных частиц, которую называют физикой высоких энергий. Для нас важно то, что кварковая структура протонов и нейтронов явно не проявляется ни в строении атомов или молекул, ни в химических процессах. Поэтому при анализе структур химических соединений и их реакций можно ограничиться только четырьмя упомянутыми типами элементарных частиц, которые наиболее важны при изучении химических соединений и их реакций; это — электроны, протоны, нейтроны и фотоны.
Электрон — легчайшая стабильная элементарная частица, массой 9,10938215(45) • 10 -31 кг, и обладающая отрицательным зарядом, равным 1,602176487(40) • 10 -19 Кл (в скобках указана точность последних цифр).
Численные значения масс, зарядов элементарных частиц и других аналогичных величин, а также мировых постоянных взяты нами из [1]. Заряд электрона является элементарным, меньше его величина заряда быть не может, а заряд любого заряженного тела должен быть кратен заряду электрона. Электрон может существовать («жить») бесконечно долгое время. Что касается размера электрона как элементарной частицы, то он до настоящего времени не определен. Считают, что размер электрона меньше 10 -18 м.
Следующая важная характеристика электрона, имеющая существенное значение для строения атомов и молекул, — собственный момент количества движения. Понятие «момент количества движения» широко используют в классической физике при описании вращений различных тел. Эта величина для вращающихся тел играет ту же роль, что и импульс для тел, движущихся поступательно. Напомним, что под импульсом (р) понимают произведение массы тела (т) на его скорость (п)

Согласно законам Ньютона импульс системы сохраняется, если на нее не действуют внешние силы.
Рассмотрим понятие момента количества движения более подробно. С этой целью обратимся к изучению вращательного движения точечной массы т вокруг центра, с которым она связана посредством нити (рис. 1.1). Предположим, что скорость точечной массы равна п. Направление этой скорости благодаря натяжению нити постоянно меняется. Если длина нити равна г, то длина окружности, по которой движется точечная масса, равна 2л7*. Отметим, что нить всегда перпендикулярна к направлению скорости частицы. По аналогии с моментом сил можно сказать, что нить играет роль плеча, а импульс частицы тх> играет роль силы. Под механическим моментом количества движения (L) понимают произведение плеча (г) на импульс (ть):

Для примера рассчитаем момент количества движения электрона, предположив, что электрон вращается вокруг ядра с линейной скоростью, равной 10 6 м/с, на расстоянии 0,053 нм от ядра (0,053 нм — среднее расстояние между электроном и ядром в атоме водорода). Используя формулу (1.2), получаем:

Рассчитанная величина дает представление о порядках величин (10~ 34 Дж • с) момента количества движения в микромире.
В отсутствие внешних воздействий момент количества движения системы сохраняется, т.е. он ведет себя так же, как и импульс. Обычно величину L изображают в виде вектора, направленного по оси вращения так, чтобы при наблюдении с конца («носика») этого вектора движение частицы происходило против часовой стрелки (рис. 1.1).

Рис. 1.1. Иллюстрация понятия «момент количества движения»
Для вращающейся частицы обычно вводят понятие частоты вращения. Под частотой вращения понимают величину, равную числу оборотов вокруг оси вращения за единицу времени tQ, в качестве которой в системе СИ избрана 1 с. Так как скорость частицы постоянна и равна v м/с, то за одну секунду частица пройдет расстояние, равное ц?0 . Учитывая, что длина окружности равна 2пг, для частоты вращения (v) получаем формулу

Размерность частоты v выражена в с -1 . Ее численное значение прямо говорит о числе оборотов, совершаемое частицей за 1 с.

Наряду с понятием частоты широко используют понятие угловой частоты (угловой скорости). Дело в том, что за один цикл точечная масса проходит угол, равный 2п радиан. Под угловой частотой или угловой скоростью (со) понимают количество радиан, проходимых частицей за единицу времени. Ясно, что угловая частота и частота вращения связаны между собой простым соотношением
Размерность угловой частоты со также равна с -1 .
Величину момента количества движения записывают через частоту вращения в виде

где через / обозначена величина, называемая моментом инерции,

Видно, что формула (1.5) аналогична формуле (1.1), которая определяет импульс тела, участвующего в поступательном движении: момент инерции является аналогом массы, а угловая частота — скорости. Заметим, что такая же аналогия существует и в выражениях для кинетической энергии вращающегося тела и тела, движущегося поступательно. Действительно, величина кинетической энергии (Е) вращающейся точечной массы может быть выражена с помощью формул (1.4)—(1.6) в виде

В последнем выражении момент инерции и угловая частота (угловая скорость) во вращательном движении также аналогичны массе и линейной скорости в поступательном.
Понятием момента инерции характеризуют не только материальные точки. Его можно распространить на тела любой формы. Для этого тело мысленно разбивают на совокупность отдельных малых масс (чем они меньше, тем точнее результат расчета), и под моментом инерции тела относительно заданной оси вращения понимают сумму


где Amj — малая масса с номером /, mi — плечо, равное длине перпендикуляра, соединяющего ось с /-й малой массой. В случае свободного вращения в отсутствие внешних сил, действующих на систему, ось вращения обязана проходить через центр масс, чтобы центр масс не менял своего положения в пространстве (или двигался равномерно и поступательно). Положение центра масс обычно определяют следующим образом. Сначала выбирают некоторую ортогональную (прямоугольную) систему координат (х, у, z) . Координаты центра масс (X, Y, Z) находят по формулам

где хр yi и Zj — положение малой массы Amj в избранной системе координат, а
представляет собой полную массу тела. Заметим, что суммирование в формулах (1.8)—(1.10) можно заменить интегрированием.
В качестве примера рассчитаем момент инерции молекулы водорода. Молекула водорода состоит из двух атомов водорода. Расстояние между протонами (R) равно 0,0741 • 10 -9 м. Ось вращения проходит перпендикулярно через середину отрезка, соединяющего ядра. Поэтому момент инерции молекулы водорода относительно данной оси вращения равен

где Ми — масса атома водорода. Порядок величины 10 -17 кг м 2 характерен для моментов инерции большинства не очень больших молекул.
Вернемся к рассмотрению собственного момента количества движения электрона. Собственный момент количества движения элементарных частиц имеет специальное название — спин, что означает вращение. Электрон обладает собственным моментом количества движения, равным

Здесь через Й обозначена фундаментальная величина, широко используемая при описании явлений микромира — постоянная Планка. Вообще говоря, в литературе используют два вида постоянных Планка, обозначаемых как й и Й. Они равны

Заметим, что для краткости обычно под спином электрона (и других частиц) понимают величину момента количества движения, выраженную в единицах Й. Например, говорят, что спин электрона равен У2, подразумевая при этом, что он равен Й/2.
Природу спина электрона объясняет квантовая электродинамика, но углубленное изучение этого вопроса в данной книге невозможно. Поэтому будем считать, что так устроен электрон.
Перейдем к рассмотрению следующих элементарных частиц.
Протон — стабильная элементарная частица массой 1,673 • 10 -27 кг (в 1836 раз больше массы электрона), обладающая положительным зарядом, равным по абсолютной величине заряду электрона. Радиус протона близок к 0,8 • 10 -15 м. Протон обладает таким же спином, как и электрон, равным Й/2.
Нейтрон — элементарная частица с массой, несколько большей (в 1,00138 раз), чем у протона, и равной 1,67492728(29)-10 -27 кг. Электрического заряда нейтрон не имеет, но момент количества движения равен также Й/2. По размеру нейтрон близок к протону.
Нейтрон и протон называются нуклонами, так как именно из них строятся ядра. Нейтрон может существовать достаточно долго только внутри ядер. Свободный нейтрон нестабилен и распадается на протон, электрон и антинейтрино. Найдено, что время полураспада свободного нейтрона равно 10,6 мин. Понятие «время полураспада» широко нами будет использоваться впоследствии. Поэтому остановимся на нем более подробно.
Под временем полураспада нестабильных частиц т1/2 (нейтронов, ядер, молекул) понимается то время, через которое в системе с нестабильными частицами остается половина исходного числа этих частиц.
Исходное число частиц должно быть при этом достаточно большим. Время полураспада т1/2 нельзя понимать так, что через два интервала 2т1/2 в системе не останется больше ни одной частицы. Чтобы понять эту особенность времени полураспада, рассмотрим другой пример. Пусть по трассе едут автомашины со скоростью 100 км/ч. В 12:00 все водители получают приказ начать равномерное торможение, причем так чтобы через 10 мин скорость упала на 50 км/ч, т.е. в два раза. Если водители выполняют этот приказ, то через 10 мин скорость машин будет равна 50 км/ч. Еще через 10 мин они остановятся.
С нейтронами дело обстоит иначе: отдельный нейтрон не может распасться наполовину. Никто не может им отдать приказ распадаться или не распадаться. Можно только говорить, что частицы имеют одинаковые шансы распасться или не распасться в какой то момент внутри промежутка времени 0-к:]/2. Но в течение следующего промежутка т1/2-5-2т1/2 шансы распасться или не распасться одинаковы, и так далее. Это означает, что несмотря на краткость времени (т1/2 = 10,6 мин) конкретный нейтрон может просуществовать годы. Следовательно, время полураспада всегда нужно относить только к достаточно большому ансамблю частиц. Если наблюдение ограни- ю
чивается только одной частицей, то она может распасться в течение первых 10 сек, но может не распасться и за год. Наблюдение только за одной частицей не информативно. Если нейтронов достаточно много, например 6 10 23 , то через 10,6 мин их будет 3 10 23 , еще через 10,6 мин — 1,5 10 23 , еще через 10,6 мин — 0,75-10 23 и т.д. Следовательно, через каждый интервал т1/2 число частиц уменьшается вдвое. Сказанное можно выразить в виде следующих формул:


и т.д.

Здесь в скобках указано время, прошедшее с начала момента наблюдения. Из приведенных равенств видно, что число частиц в момент времени тт1/2 станет равным
Полученная формула верна для любых значений т, не обязательно целых. Таким образом, для любого момента времени t можно узнать значение т, т.е. узнать какое значение времени t составляет в единицах т1/2, а затем рассчитать, сколько частиц останется в системе


Обычно полученный закон случайного распада записывают через экспоненциальную показательную функцию, в качестве основания которой используют не число 2, а число е = 2,718281828. . Тогда (1.13) можно преобразовать, записав число 2 в виде е 1п2 , находим

Кривая N(t)/ Л г (0)изображена на рис. 1.2.
Вспоминая, чему равно т, получаем

Последнюю формулу часто записывают так:

где величина т носит название времени жизни, а величина к — константы скорости распада. Время жизни показывает, какой отрезок

Рис.1.2. Зависимость N(t)/ N(0) от т для случайного самопроизвольного
времени необходим, чтобы количество частиц уменьшилось в «е» раз. Величины т и т1/2 связаны соотношением

Константу скорости распада к определяют через т:

Выражение (1.15) носит совершенно общий характер и широко используется при описании самых различных случайных процессов. В частности, оно описывает закон радиоактивного распада. Отметим, что чем больше значение к, тем меньше время полураспада и тем быстрее происходит распад.
Фотон — элементарная частица электромагнитного поля. Электромагнитное поле представляет собой совокупность электрического и магнитного полей, напряженность и ориентация которых меняются во времени и в пространстве строго определенным образом.
К электромагнитному полю относятся свет и радиоволны. Существование фотонов означает, что электромагнитное поле имеет двойственную (дуальную) природу и его можно представлять либо как совокупность электромагнитных волн, либо как совокупность фотонов. Фотоны не похожи на частицы, рассмотренные нами ранее. Они движутся в вакууме со скоростью света и не обладают массой покоя. Энергия отдельных фотонов Е прямо связана с частотой электромагнитного поля v соотношением, предложенным М. Планком

Энергию квантов света часто выражают в единицах, называемых электрон-вольтами (сокращенно — эВ). 1 эВ — это энергия, которую приобретает электрон, проходя разность потенциалов, равную 1 В. Выразим эту единицу через джоули:


Например, энергия квантов красного света составляет около 2 эВ, зеленого — 2,5 эВ, ультрафиолетового — около 4 эВ. Таким образом, все видимое человеком световое излучение является электромагнитным полем, энергии квантов которого лежат в очень узком диапазоне — 2-И- эВ.
Почему атомы — величайшее чудо Вселенной

Один из самых удивительных фактов нашего существования был впервые постулирован более 2000 лет назад: на каком-то уровне каждая часть нашей материальной реальности может быть сведена к ряду крошечных компонентов, сохраняющих свои важные индивидуальные характеристики, которые позволяют им собираться воедино и создавать все, что мы видим, знаем, встречаем и переживаем. Эта простая мысль, приписываемая Демокриту Абдерскому, со временем переросла в атомистическое представление о Вселенной.
Хотя буквальное греческое слово «ἄτομος», означающее «неразрезаемый», не совсем применимо к атомам, поскольку они состоят из протонов, нейтронов и электронов, любая попытка «разделить» атом дальше приводит к потере его сущности: того факта, что он является определённым, конкретным элементом таблицы Менделеева. Именно это свойство позволяет ему создавать все те сложные структуры, которые существуют в нашей наблюдаемой реальности: количество протонов, содержащихся в атомном ядре.
Атом настолько мал, что если подсчитать общее количество атомов, содержащихся в одном человеческом теле, то получится около 10 28 : это более чем в миллион раз больше, чем количество звёзд во всей видимой Вселенной. И всё же сам факт того, что мы состоим из атомов, является, пожалуй, величайшим чудом во всей Вселенной.
В атоме, молекуле или ионе переход электронов с более высокого энергетического уровня на более низкий приводит к испусканию излучения с совершенно определённой длиной волны, определяемой фундаментальными константами. Если эти константы изменятся, то изменятся и свойства атомов во всей Вселенной.
Простой факт: именно скромный атом лежит в основе всего известного нам вещества во Вселенной — от обычного газообразного водорода до человека, планет, звёзд и т.д. Все, что состоит из обычной материи в нашей Вселенной — твёрдое, жидкое или газообразное — состоит из атомов. Даже плазма, возникающая в условиях очень высоких энергий или в разреженных глубинах межгалактического пространства, — это просто атомы, лишённые одного или нескольких электронов. Атомы сами по себе очень простые образования, но даже при таких простых свойствах они могут собираться в сложные комбинации, которые просто поражают воображение.
Поведение атомов поистине удивительно. Рассмотрим следующие факты:

- Они состоят из небольшого массивного положительно заряженного ядра, вокруг которого вращается большое маломассивное рассеянное облако отрицательно заряженных электронов.
- При приближении друг к другу атомы поляризуются и притягиваются, в результате чего они либо обмениваются электронами (ковалентно), либо один атом отбирает у другого один или несколько электронов (ионно).
- Когда несколько атомов связываются друг с другом, они могут образовывать молекулы (ковалентно) или соли (ионно), которые могут быть как простыми, состоящими всего из двух атомов, так и сложными, состоящими из нескольких миллионов атомов.
Молекулы — примеры частиц вещества, связанных в сложные конфигурации, — приобретают такие формы и структуры в основном благодаря электромагнитным силам, существующим между входящими в их состав атомами и электронами. Разнообразие доступных структур практически безгранично.
Существует два ключа к пониманию того, как взаимодействуют атомы.

- Каждый атом состоит из электрически заряженных компонентов: положительно заряженного ядра и ряда отрицательно заряженных электронов. Даже когда заряды статичны, они создают электрические поля, а когда заряды находятся в движении, они создают магнитные поля. В результате каждый существующий атом может стать электрически поляризованным при попадании в электрическое поле, а каждый существующий атом может стать намагниченным при воздействии магнитного поля.
- Электроны, вращающиеся вокруг атома, будут занимать самый низкий доступный энергетический уровень. Хотя электрон может находиться в любой точке пространства в пределах примерно 0,1 нанометра от атомного ядра, он может занимать только определённый набор значений энергии, диктуемый правилами квантовой механики. Распределения вероятности нахождения электронов в зависимости от энергетического уровня также определяются правилами квантовой механики и подчиняются определённому распределению вероятности, которое однозначно вычисляется для каждого типа атомов с любым произвольным числом связанных с ними электронов.
Уровни энергии и волновые функции электронов, соответствующие различным состояниям в атоме водорода (хотя эти конфигурации чрезвычайно похожи у всех атомов). Уровни энергии квантованы в кратных значениях постоянной Планка, но размеры орбиталей и атомов определяются энергией основного состояния и массой электрона. В силу принципа исключения Паули на каждом из этих энергетических уровней могут находиться только два электрона, с одним верхним и одним нижним спином, в то время как другие электроны должны занимать более высокие и объёмные орбитали. При переходе с более высокого энергетического уровня на более низкий необходимо изменить тип орбитали, на которой находится электрон, если он собирается испустить только один фотон, иначе он нарушит определённые законы сохранения.
В очень хорошем приближении наше представление о материи во Вселенной, заключающиеся в том, что она состоит из атомов с тяжёлым, положительно заряженным ядром и лёгкими, отрицательными зарядами вокруг него, которые поляризуются в ответ на электрические поля и намагничиваются в ответ на магнитные поля, которые могут обмениваться (ионно) или делиться (ковалентно) электронами с другими атомами, образуя связи, вызывая поляризацию и намагничивание и воздействуя на другие атомы вокруг себя, может объяснить практически всё в нашей привычной, повседневной жизни.
Атомы соединяются друг с другом, образуя молекулы: связанные состояния атомов, которые складываются в почти бесчисленное множество конфигураций и могут взаимодействовать друг с другом самыми разнообразными способами. Соедините вместе большое количество аминокислот — и вы получите белок, способный выполнять ряд важных биохимических функций. Добавьте к белку ион — и вы получите фермент, способный изменять структуру связей в различных молекулах.
А если выстроить цепочку нуклеиновых кислот в правильном порядке, то можно закодировать как создание произвольного количества белков и ферментов, так и создание копий самого себя. При правильной конфигурации собранный набор атомов будет составлять живой организм.

Хотя человек состоит из клеток, на более фундаментальном уровне мы состоим из атомов. Всего в человеческом теле насчитывается около ~10 28 атомов, по количеству в нас больше всего водорода, а по массе — кислорода и углерода.
Если бы всё человеческие знания когда-нибудь были уничтожены в результате грандиозного апокалипсиса, но остались бы выжившие разумные люди, то простая передача им знаний об атомах помогла бы им не только разобраться в окружающем мире, но и начать путь к восстановлению законов физики и всего комплекса поведения материи.
Знание об атомах очень быстро приведёт к реконструкции периодической таблицы. Понимание того, что в микроскопическом мире есть, на что посмотреть, привело к открытию клеток, органелл, а затем и молекул и их атомных составляющих. Химические реакции между молекулами и связанные с ними изменения конфигураций привели к открытию как способов хранения энергии, так и способов её высвобождения, как биологических, так и неорганических.
То, на что у человеческой цивилизации ушли сотни тысяч лет, может быть открыто за одну человеческую жизнь, и это даст увлекательные намёки на будущее, когда будут открыты такие свойства, как радиоактивность или возможности взаимодействия света и материи.

Периодическая таблица элементов отсортирована таким образом (по периодам, напоминающим строки, и группам, напоминающим столбцы) из-за количества свободных/занятых валентных электронов, что является фактором номер один, определяющим химические свойства каждого атома. Атомы могут соединяться в молекулы в огромном количестве, но именно электронная структура каждого из них в первую очередь определяет, какие конфигурации возможны, вероятны и энергетически благоприятны. До 2003 г. висмут считался самым тяжёлым стабильным элементом, а сегодня мы знаем, что он нестабилен по своей природе.
Но атом — это ещё и достаточный ключ к выходу за рамки дальтоновского представления о мире. Открытие того, что атомы могут иметь разную массу, но при этом сохранять свои элементарные свойства, привело бы не только к открытию изотопов, но и помогло бы исследователям обнаружить, что атомные ядра состоят из двух различных типов частиц: протонов (с положительным зарядом) и (незаряжённых) нейтронов.
Это более глубокое открытие, чем может показаться на первый взгляд. Внутри атомного ядра существуют два типа составных частиц с почти, но не совсем одинаковыми массами, причём более лёгкая имеет положительный заряд, а более тяжёлая – нейтральный. Вокруг всего ядра вращаются электроны — частицы, имеющие одинаковый с протоном заряд и меньшую массу, чем разница масс протона и нейтрона внутри ядра.
Если взять свободный протон, то он будет стабилен. Если взять свободный электрон, то он тоже будет стабильным. А если взять свободный нейтрон, то он не будет стабильным, а распадётся на протон, электрон и (возможно) третью, нейтральную частицу.

Схематическая иллюстрация ядерного бета-распада в массивном атомном ядре. Бета-распад — это распад, протекающий через слабые взаимодействия с превращением нейтрона в протон, электрон и антиэлектронное нейтрино. Среднее время жизни свободного нейтрона составляет около 15 минут, но связанные нейтроны могут быть стабильными до тех пор, пока мы их измеряем.
Это небольшое осознание, внезапно пришедшее в голову, могло бы научить вас огромному количеству знаний о фундаментальной природе реальности.
Во-первых, оно сразу же подскажет вам, что между протонами и/или нейтронами должно существовать какое-то дополнительное взаимодействие, отличное от электромагнитной. Например, существование дейтерия (изотопа водорода с 1 протоном и 1 нейтроном) говорит нам о том, что между протонами и нейтронами существует некая сила притяжения, которую нельзя объяснить ни электромагнетизмом (поскольку нейтроны нейтральны), ни гравитацией (поскольку гравитационные силы слишком слабы, чтобы объяснить такое связывание). Должна существовать какая-то ядерная сила, связывающая нейтроны.
Эта сила должна, по крайней мере, на некотором небольшом расстоянии преодолевать электростатическое отталкивание между протонами внутри одного атомного ядра: другими словами, она должна быть сильнее, чем даже (достаточно сильная сама по себе) сила отталкивания между двумя протонами. Поскольку стабильных атомных ядер, состоящих только из двух (или более) протонов, не существует, нейтрон должен играть определённую роль в стабильности ядра.
Другими словами, уже одно открытие того, что атомные ядра содержат и протоны, и нейтроны, делает необходимым существование сильного ядерного взаимодействия — или чего-то очень похожего на неё.
Отдельные протоны и нейтроны могут быть «бесцветными» образованиями, но кварки, входящие в их состав, «цветные». Глюоны могут обмениваться не только между отдельными глюонами внутри протона или нейтрона, но и в комбинациях между протонами и нейтронами, что приводит к ядерному связыванию. Однако каждый такой обмен должен подчиняться полному набору квантовых правил.
Кроме того, как только человек обнаружит, что свободный нейтрон может распадаться, или обнаружит радиоактивный бета-распад, или обнаружит, что звёзды питаются за счёт ядерного синтеза в их ядрах, он сразу же сможет сделать вывод о существовании четвёртого фундаментального взаимодействия в дополнение к гравитации, электромагнетизму и сильному ядерному взаимодействию: того, что мы называем слабым ядерным взаимодействием.
Должно существовать взаимодействие, позволяющее взять несколько протонов, слить их вместе, а затем перевести в состояние, менее массивное, чем исходные два протона, где один протон превращается как минимум в нейтрон и позитрон (антиэлектрон), и при этом сохраняются энергия и импульс. Способность превращать один тип частиц в другой, отличающийся от «суммы частей» или от «создания равных количеств материи и антиматерии», — это то, чего нельзя достичь при помощи трёх других взаимодействий. Просто изучая атомы, можно сделать вывод о существовании слабого ядерного взаимодействия.

Наиболее простая и низкоэнергетическая версия протон-протонной цепочки, в которой из исходного водородного топлива получается гелий-4. Отметим, что только при слиянии дейтерия и протона из водорода получается гелий; во всех остальных реакциях либо образуется водород, либо гелий получается из других изотопов гелия.
Для того чтобы существовала Вселенная с большим количеством типов атомов, необходимо, чтобы наша реальность обладала определённым набором свойств.
- Протон и нейтрон должны быть очень близки по массе: настолько близки, что у связанного состояния протона и нейтрона, т.е. у дейтрона масса должна быть меньше, чем у двух протонов по отдельности.
- Электрон должен быть менее массивным, чем разница масс протона и нейтрона, иначе нейтрон был бы абсолютно стабилен.
- Более того, электрон должен быть намного, намного легче протона или нейтрона. Если бы он имел сравнимую массу, то атомы были бы не только намного меньше (вместе со всеми связанными с ними структурами, построенными из атомов), но электрон проводил бы так много времени внутри атомного ядра, что спонтанная реакция слияния протона с электроном с образованием нейтрона была бы быстрой и вероятной, а соседние атомы спонтанно сливались бы друг с другом даже в условиях комнатной температуры. (Мы видим это на примере мюонного водорода, созданного в лаборатории).
- И, наконец, уровни энергии, достигаемые в звёздах, должны быть достаточными для того, чтобы атомные ядра внутри них подверглись ядерному синтезу, но не может быть так, что всё более тяжёлые атомные ядра всегда более стабильны, иначе мы получили бы Вселенную, заполненную сверхтяжёлыми и сверхкрупными атомными ядрами.
Существование Вселенной, богатой разнообразными атомами, но с преобладанием водорода, требует наличия всех этих факторов.

Анатомия очень массивной звезды на протяжении всей её жизни, кульминацией которой является сверхновая типа II (с коллапсом ядра), когда в ядре заканчивается ядерное топливо. На последней стадии термоядерного синтеза, как правило, происходит горение кремния, в результате чего в ядре на короткое время образуется железо и железоподобные элементы, после чего возникает сверхновая. Наиболее массивные сверхновые с коллапсом ядра обычно приводят к образованию чёрных дыр, а менее массивные — только нейтронных звёзд.
Если бы разумное существо из другой Вселенной впервые столкнулось с нами и нашей реальностью, то, возможно, первое, что мы хотели бы донести до него, — это то, что мы состоим из атомов. Что внутри всего, что состоит из материи в этой Вселенной, есть крошечные, маленькие образования — атомы, которые сохраняют основные свойства, присущие только данному виду атомов. Можно варьировать массу ядер внутри этих атомов и получить один и тот же вид атома, но если изменить их заряд, то получится совершенно другой атом. И что все эти атомы вращаются по орбитам с таким количеством отрицательно заряженных электронов, которое необходимо для точного уравновешивания положительного заряда в ядре.
Изучая поведение и взаимодействие этих атомов, мы можем понять практически все молекулярные и макроскопические явления, возникающие на их основе. Рассматривая внутренние компоненты этих атомов и то, как они собираются, мы можем узнать о фундаментальных частицах, силах и взаимодействиях, которые лежат в основе нашей реальности. Если бы существовала только одна информация, которую можно было бы передать выжившей группе людей в постапокалиптическом мире, то, возможно, ни одна информация не была бы столь ценной, как тот факт, что все мы состоим из атомов. В каком-то смысле это самое чудесное свойство из всех, относящихся к нашей Вселенной.
- Научно-популярное
- Физика