Атом можно представить как конструктор «Лего», который можно собрать из более простых “элементарных” частиц. У каждого атома число “деталек” может быть различным. Об этом и о других особенностях строения атома поговорим в статье.
Великие ученые и философы древности упорно бились над вопросом, из чего же состоят вещества, которые их окружают. Впервые идею о том, что все тела живой и неживой природы состоят из мельчайших частиц — атомов — высказал древнегреческий ученый Демокрит целых 2500 лет назад!
Что же из себя представляет атом?
Атом — это мельчайшая химически неделимая частица вещества.
Атомы могут соединяться друг с другом с помощью химических связей в различной последовательности, образуя более сложные частицы — молекулы. Можно провести аналогию:
- атом — отдельный человек,
- молекулы — группы людей, объединенные общим признаком (семья, одноклассники, коллеги, любители кошек, любители собак).
Молекула — это мельчайшие частицы, которые состоят из атомов. Они являются химически делимыми.
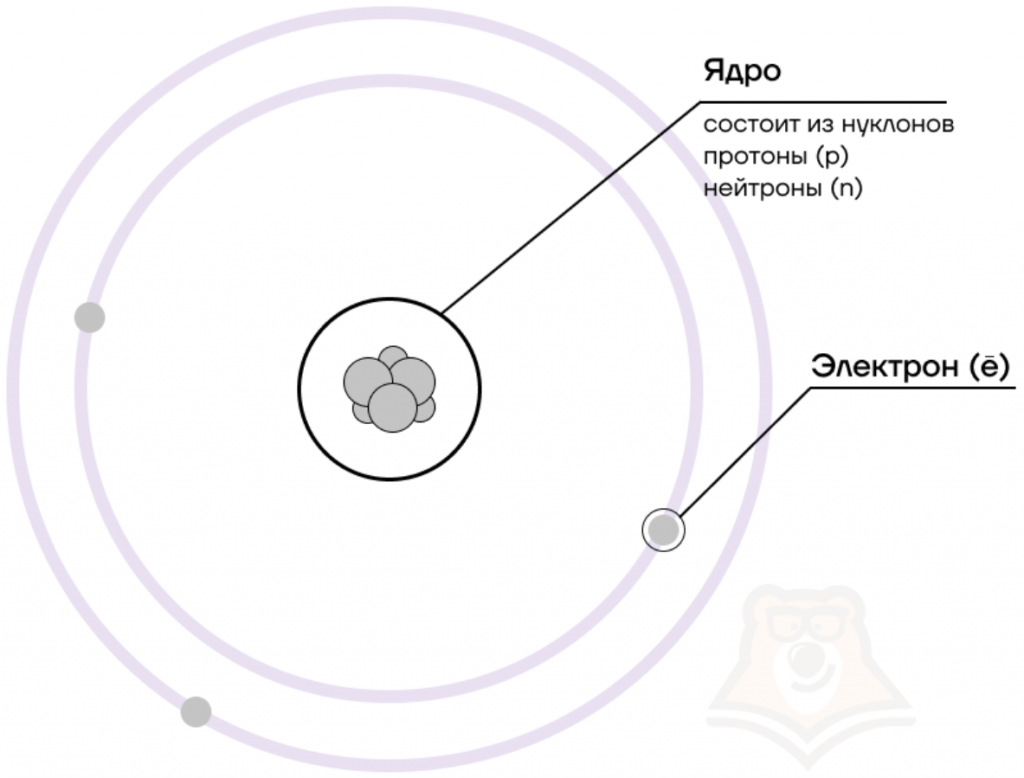
Долгое время считалось, что атом нельзя разделить далее на составляющие. Но с развитием науки учёные-физики выяснили, что атом состоит из более мелких, или элементарных частиц — протонов (p), нейтронов (n) и электронов (ē).
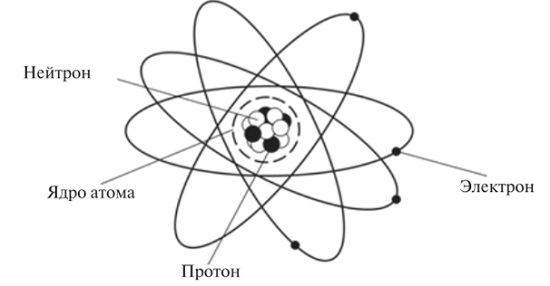
В центре атома располагается ядро, которое состоит из протонов и нейтронов (их общее название нуклоны), а вокруг ядра вращаются электроны.
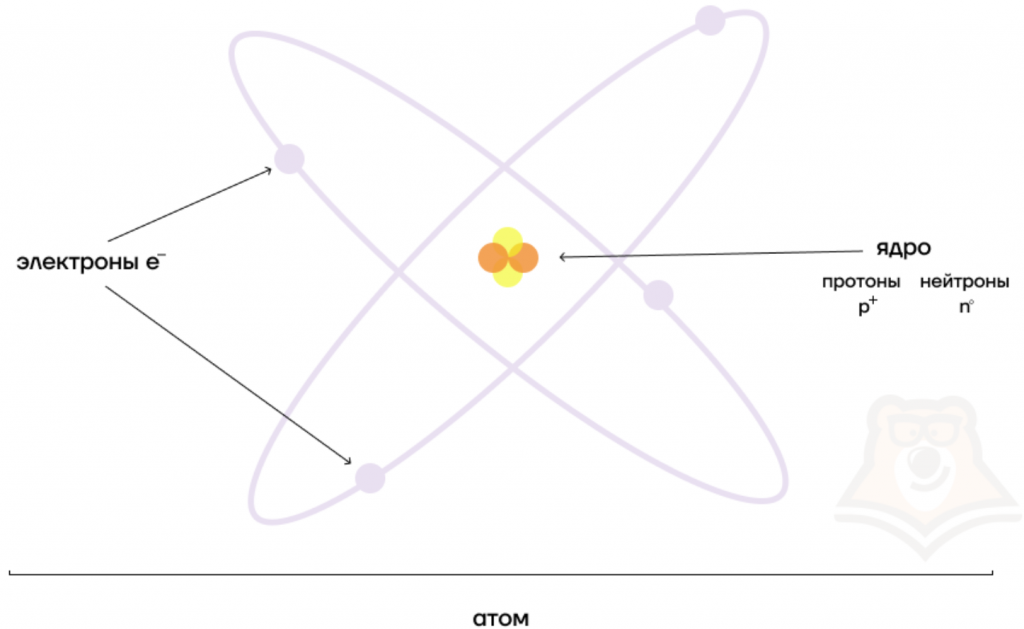
| Чем атом похож на Солнечную систему? Можно представить атом как Солнечную систему, где вокруг ядра (Солнца) по орбитам вращаются электроны (планеты). Это так называемая планетарная модель атома. В реальности атом намного сложнее, но для запоминания нам удобнее пользоваться этими представлениями. |
Тогда более точно определение атома будет звучать так:
Атом — электронейтральная химически неделимая частица, которая состоит из положительно заряженного ядра и вращающихся вокруг него отрицательно заряженных электронов.
Каждая из элементарных частиц в атоме имеет свой заряд и массу:

Характеристика элементарных частиц
Из таблички видно, что вся масса атома сосредоточена в протонах и нейтронах, то есть в ядре. При этом само ядро положительно заряжено, а вокруг ядра вращаются отрицательно заряженные электроны.
В разновидностях одного и того же химического элемента может быть различное число элементарных частиц. Давай рассмотрим это на примере атома водорода.
Строение атомов. Протоны, нейтроны, электроны. Химия 8 класс

Первый случай: ядро атома водорода состоит из одного протона (масса ядра = 1 а.е.м.). Такой атом называется протием, именно он указан в периодической системе Д.И. Менделеева.
Добавим к этому ядру один нейтрон, тогда масса ядра будет равна 2 а.е.м.. Мы получили вторую разновидность атома водорода — дейтерий.
Если добавить второй нейтрон к такому ядру, то мы получим тритий. Так вот, разновидности одного и того же химического элемента, которые различаются числом нейтронов в ядре, называются изотопами.
Атом. Ион
Текст является частью пособия по химии.
Автор текста – Анисимова Елена Сергеевна. https://vk.com/bch_5
Авторские права защищены. При копировании и передаче текста указание автора и ссылка на ВК обязательны.
Распространение и изучение текста приветствуется. – Давайте станем более информированными.
Курсивом набран текст пояснений, напоминаний или фактов на будущее. При первом чтении или спешке его можно не читать.
Справа расположены рекомендации.
Параграф 1: Элементарные частицы
Параграф 2: Атом
Параграф 3: Ионы
Параграф 1: Элементарные частицы
В природе есть вещицы, которые называют:
протонами, электронами и нейтронами.
Эти частицы относятся к элементарным частицам.
Эти три – основные, но есть и множество других.
Элементарные частицы очень маленькие по размерам, он не видны в микроскопы.
Масса элементарных частиц
Кратко: масса протона и нейтрона – по 1, масса электрона почти ноль.
Масса протона равна условной единице.
(См. определение атомной единицы массы).
Масса нейтрона почти равна массе протона, то есть тоже единице.
Масса электрона не ноль, но в 1836 раз меньше протона, и часто не учитывается.
Оформим эти сведения в виде маленькой таблицы для упрощения усвоения:
Протон Нейтрон Электрон
Масса 1 1 Почти 0
Заряды элементарных частиц (электрические заряды)
Кратко: заряд нейтрона – ноль, протона – плюс 1, электрона – минус 1.
Что такое электрический заряд?
Существует такое свойство тел, которое называют электрическим зарядом.
Наличие электрического заряда проявляется в способности реагировать на другие предметы, имеющие электрический заряд.
Реакция (заряженного тела на заряд другого) проявляется в том, что предмет, имеющий электрический заряд,
— или притягивается к другому заряженному предмету,
— или отталкивается от него.
Типы эл. зарядов.
Заряд бывает двух типов – один тип эл. заряда назван положительным, а другой тип – отрицательным.
Принято говорить, что положительный и отрицательный – разноимённые.
Положительный заряд притягивается к отрицательному (то есть разноимённые заряды притягиваются). Точнее, тела с такими зарядами.
Положительный от положительного отталкивается, отрицательный от отрицательного тоже отталкивается.
(То есть одноимённые отталкиваются – точнее, тела с одноимёнными зарядами).
Заряд нейтрона
У нейтрона нет электрического заряда, то есть он электронейтрален (отсюда и его название – нейтрон). То есть нейтрон не реагирует на частицы с эл. зарядом.
Заряды протона и нейтрона
У протона и электрона есть электрические заряды –
равные по величине, но противоположные по «знаку». –
Заряд протона считается положительным,
а заряд электрона считается отрицательным.
Величина заряда
Величина заряда протона или электрона принята за условную единицу.
Суммарный заряд протона и электрона равен нулю. (Сумма электро-нейтральна).
(Плюс один и минус один в сумме дают ноль.)
Когда число протонов равно числу электронов, то суммарный заряд равен нулю.
Если число протонов больше или меньше числа электронов – заряд не нулевой.
Таблицы «Заряды элементарных частиц»:
Протон Электрон Нейтрон
Заряд Плюс 1 Минус 1 0
Обобщение по свойствам элементарных частиц.
Таким образом, у нейтрона нет заряда, а у электрона почти нет массы.
Массы протона и нейтрона – по единице.
Заряды протона и электрона – по единице.
Свойства протона: масса 1 и заряд +1.
Свойства нейтрона: масса 1 и заряд 0.
Свойства электрона: масса 0 и заряд –1.
Обобщим сведения об основных свойствах элементарных частиц в таблице:
«Свойства элементарных частиц»
Протон Электрон Нейтрон
Масса 1 0 1
Заряд Плюс 1 Минус 1 Ноль
(нет заряда)
Это очень простые сведения.
Но из них есть множество важных выводов.
Из них выводится множество фактов. Так что эту таблицу – знать.
Элементарные частицы в природе
Потоки протонов и электронов распространяются от Солнца по всей Солнечной системе!
В каком виде существуют элементарные частицы в природе?
В «свободном виде» протоны и электроны есть в Солнце и многих других звёздах.
От Солнца протоны и электроны распространяются прочь от Солнца – по Солнечной системе. Этот поток заряженных частиц называют солнечным ветром.
Солнечный ветер оказывает влияние на жизнь людей:
он может приводить к сбоям техники, электроники, связи!
А если бы не атмосфера (воздушная оболочка Земли), то солнечный ветер мог бы погубить живые организмы Земли!
Но на Земле протоны, электроны и нейтроны обычно объединяются,
образуя системы: а-то-мы. (См. также ионы).
В космосе атомы тоже есть – в молекулярных облаках между звёздами.
Параграф 2: Атом
Протоны, электроны и нейтроны существуют в природе обычно не по отдельности,
а объединяются в единые системы.
Часто система из элементарных частиц содержит одинаковое число протонов и электронов.
Такая система из равного числа протонов и электронов называется атомом.
Атом тоже считается частицей, но уже не элементарной.
Атом – ключевое понятие в науках о веществах.
Часто в атоме есть и нейтроны. –
Иногда нейтронов в атоме столько же, сколько и протонов, иногда меньше (у протия), а иногда нейтронов намного больше, чем протонов; чем больше в атоме протонов – тем больше и нейтронов на долю протонов.
Протоны и электроны могут входить в состав единой системы,
которая называется атомом.
(Если протонов и электронов поровну).
Как уже сказано, число протонов и электронов в атоме всегда равное.
Из-за этого суммарный заряд протонов (он равен числу протонов со знаком плюс)
и суммарный заряд электронов (он равен числу электронов со знаком минус)
в сумме дают ноль – нейтральный заряд атома как целого или просто отсутствие заряда у атома.
Параграф 3: И-о-ны
Некоторые атомы могут присоединять к себе «лишние» электроны.
Некоторые атомы могут терять свои электроны (обычно от 1 до 7).
После потери электрона или присоединения электронов заряд атома перестаёт быть нулевым, и атом уже не атом!
Если атом теряет электрон или присоединяет к себе электрон, то он:
перестаёт быть нейтральным, перестаёт считаться атомом,
и получает название ИОН.
Ион не является нейтральной частицей.
Ион всегда имеет заряд, в отличие от атома.
Ион – это бывший атом; зарядившийся атом.
Атом плюс или минус электрон(ы) = ион
Но. Зарядившиеся молекулы тоже называют ионами – см. далее!
Какие бывают ионы…
Если атом теряет электроны (а вместе с ними и отрицательные заряды),
то в возникшем ионе:
имеется дефицит отрицательных зарядов (по сравнению с бывшим атомом),
что даёт иону положительный заряд.
Кратко: потеря электронов атомом превращает его в положительный ион (катион).
Атом минус электрон(ы) = ион с положительным зарядом (катион)
Если атом присоединяет к себе электроны (и отрицательный заряд вместе с ними),
то в возникшем ионе имеется избыток отрицательных зарядов.
Кратко: приобретение электронов атомом превращает его в отрицательный ион (анион).
Атом плюс электрон(ы) = ион с отрицательным зарядом (анион)
Явление превращения атома в ион (в результате присоединения электрона или потери электрона) называется ионизацией.
Где встречаются ионы
Ионы есть везде – на Земле, в воле, почве, воздухе, организме.
В Солнце в основном ионы, а атомов мало или нет, то есть вещество в ионизированном состоянии.
Типы атомов
Сколько бывает протонов в атомах?
Об этом – в файле «Типы атомов. Химические элементы».
Массы трех фундаментальных частиц, выраженные в а.е.м., имеют следующие значения:
масса протона – 1.007277 а.е.м., масса нейтрона – 1.008665 а.е.м., масса электрона – 0.000548 а.е.м.
Указывать массу электрона 0- принципиальная ошибка,вводит учеников в дальнейшие заблуждения.
Электрон протон нейтрон это
Из курса химии средней школы вы знаете, что атом состоит из ядра и электронной оболочки. Ядро состоит из нуклонов — протонов и нейтронов, электронная оболочка — из электронов. Эти частицы называются элементарными.
В целом атом электронейтрален, так как заряды ядра и электронной оболочки компенсируют друг друга: число протонов в ядре равно числу электронов в электронной оболочке.
Таблица 1. Основные характеристики элементарных частиц
* Величина заряда электрона и протона равна `1,60*10^(-19)` Кл.
Масса атома в основном сосредоточена в ядре и определяется суммой масс протонов и нейтронов, т. к. электроны из-за своей малой массы на эту величину практически не влияют.
Сумма масс протонов и нейтронов называется массовым числом. При обозначении элемента она ставится как левый верхний индекс: $ <>_<>^mathrm$.
Заряд ядра
важнейшая характеристика атома, лежащая в основе его современного определения.
В Периодической системе Д.И. Менделеева порядковый номер элемента определяется именно зарядом ядра.
При обозначении элемента он ставится как левый нижний индекс.
Изотопы
Атомы с одинаковым зарядом ядра могут иметь разное количество нейтронов, то есть разные массы. Разновидности атомов одного и того же химического элемента, имеющие одинаковый заряд ядра, но разные массы, называют изотопами.
Изотопы одного и того же элемента имеют одинаковые химические свойства, так как масса атома не играет существенной роли непосредственно в формировании этих свойств.
Электроны
Частицы, которые вращаются в облачном пространстве вокруг ядра, настолько малы, что их размеры смогла установить только лишь квантовая механика. Ученые доказали, что электроны фундаментальные частицы, их состав в атоме может меняться. Тогда атом становится несбалансированным, меняет заряд. Если заряд становится положительным, то атом называют катионом, если отрицательным, то анионом.
На изменение свойств атома влияет излучение энергии. Этот процесс называют ионизирующим излучением.
Мельчайшие частицы атома: основа электротока
Взаимодействие частиц объясняет механизм электрического тока. Он представляет собой поток электронов, проходящих через вещества проводники.
Поток возможен, когда электроны разрывают атомную связь. Разрыв происходит под воздействием энергии, она дает возможность электрону преодолеть электромагнитные силы, которые его сдерживают. В материалах, относящихся к проводникам, электроны имеют свободную связь с ядрами, поэтому требуется минимальное количество энергии для их движения.
Потоки электронов можно генерировать с помощью специальных устройств, генераторов, работающих на основе принципа электромагнитной индукции. Также процесс генерации возможен под воздействием химических реакций и световой энергии.
- Винипласт
- Гетинакс
- Доставка товаров из Китая
- Изолента
- Изофлекс 191
- Капролон
- КИФЭ слюдопласт
- Лак МЛ-92
- Лакоткань
- Лауретсульфат натрия (SLES 70%)
- Лента киперная
- Лента ЛСКЛ-155
- Лента ЛЭТСАР
- Лента слюдинитовая
- Лента смоляная
- Лента стеклобандажная ЛСБЭ
- Лента стеклянная ЛЭС
- Лента тафтяная
- Лента ФУМ
- Миканиты
- Оргстекло
- Пластикат 57-40
- Пленка полиимидная ПМ-А
- Пленка ПЭТ-Э
- Пленкосинтокартон ПСК
- Пленкоэлектрокартон ПЭК
- Полиацеталь ПОМ
- Полиуретан
- Полиэтилен PE-1000
- Провод БПВЛ
- Провод ПВ-3 (ПУГВ)
- Стеклолакоткань
- Стекломиканит гибкий
- Стеклопластик UPM-203 (полный аналог Durostone)
- Стеклотекстолит
- Стеклотекстолит фольгированный FR-4
- Стеклоткань
- Текстолит
- Трубка ТВ-40
- Трубка ТКР
- Трубка ТЛВ
- Трубка ТУТ
- Трубка фторопластовая Ф-4Д
- Фторолакоткань Ф-4Д
- Фторопласт
- Шнуры электроизоляционные
- Электрокартон
- Эмалированный провод
- Эмаль ГФ-92 ХС
Атом — его состав и структура
Атом — основная единица элементов. Состав атома и его строение определяет различные свойства элементов. Например, состав атома кристалла кремния будет отличаться от структуры, что представляет, например, вещество уран.
Слово «атом» происходит от греческих корней «а»(без) и «том» (вырезать) что означает «неделимый». Вплоть до 20-го века атомы считались минимально возможными частицами.
Ядро является центральным, очень плотным компонентом атома. Оно состоит из протонов и нейтронов (совместно называемых нуклонами) и отвечает за большую часть атомной массы. Протоны и нейтроны удерживаются вместе в ядре так называемым сильным ядерным взаимодействием (которое является самой сильной известной силой во Вселенной). Вокруг ядра находится облако гораздо меньших и более легких электронов, которые притягиваются к ядру электромагнитной силой от взаимодействия с протонами. Различные количества протонов, нейтронов и электронов приводят к тому, что атом обладает различными химическими свойствами, которые определяют, что это за элемент. Атомы невообразимо малы, а их ядра в 1000 раз меньше. На самом деле один кубический сантиметр кремния, содержит приблизительно 5 х 10 22 атома (это 5 с 22 нулями после него!). Это масштабы Вселенной, чтобы увидеть визуальное представление о том, насколько они малы.
Протоны
Протоны — это положительно заряженные частицы, которые находятся внутри ядра атома.
Элемент можно распознать по числу протонов в ядре одного из своих атомов. Кроме того, число протонов определяет место элемента в периодической таблице элементов. Например, состав атома углерода имеет ровно 6 протонов в своем ядре и, таким образом, номер 6 в периодической таблице элементов, торий имеет ровно 90 протонов и, таким образом, номер 90 в периодической таблице элементов.
Протоны отталкиваются друг от друга электромагнитной силой, но стягиваются вместе сильной силой, которая сильнее на коротких расстояниях (эти расстояния составляют около ферми или 10-15 м). Протоны очень маленькие, около 10-15 м в 10 000 раз меньше атома! Несмотря на свои невероятно малые размеры, протоны толкают друг друга с огромной силой, около 100 Н, сравнимой с весом маленькой собаки!
Заряд протона в точности равен и противоположен заряду электрона. Поэтому число электронов в нейтральном атоме всегда равно числу протонов. Протоны состоят из более мелких частиц, называемых кварками, которые также составляют нейтроны.
Число протонов в ядре называется атомным номером, и это число определяет, каким элементом является вещество. Другими словами, изменение числа протонов, изменяет элемент. Это число протонов (атомный номер) изменяется, когда ядро подвергается бета-распаду или альфа-распаду в любой из его различных форм.
Сложность намеренного изменения количества протонов в ядре велика. Вот почему алхимия (средневековая практика превращения свинца в золото) так долго терпит неудачу!
Нейтроны
Нейтроны имеют ту же массу, что и протоны, что делает их легко определяемыми, сколько находятся в составе ядра атома.
Простое вычитание числа протонов из атомной массы атома даст число нейтронов. Например, цезий является номером 55 в периодической таблице элементов и, следовательно, имеет 55 протонов; кроме того, его атомная масса (обычно также найденная в периодической таблице), как известно, составляет 133 (единицы атомной массы). Вычитание 55 из 133 дает 78, то есть число нейтронов в атоме. Один и тот же тип атома (определяемый количеством протонов) может иметь разное количество нейтронов. Они называются различными изотопами атома. Например, углерод-12 является одним изотопом углерода, а углерод-14 — другим изотопом углерода. Имеется общее название составляющих атомного ядра. Нуклон — частица из протона и нейтрона, которые образуют ядро. Нуклиды — совокупность атомов с определенным значением нейтронов и протонов: одинаковое число протонов, но разным числом нейтронов. Нуклоны и нуклиды разные понятия.
Электроны
Электроны — это отрицательно заряженные частицы, которые существуют в облаке вокруг ядра атома. Они невообразимо малы, настолько малы, что квантовая механика необходима для объяснения их специфического поведения, и насколько физика смогла определить, они являются фундаментальной частицей. Лучше всего представить электроны как крошечные частицы, которые» вращаются » вокруг ядра. Их радиус настолько мал, что никто не смог его обнаружить, но он невероятно круглый. Если бы электрон был увеличен до размера Солнечной системы, он все равно выглядел бы сферическим в пределах толщины человеческого волоса.
- Масса 9.11×10 -31 кг
- Радиус менее 10 -18 м
- Отклонение от сферы менее 10 -26 м
Состав атома определяет одинаковое количество протонов и электронов, однако он может потерять или приобрести электрон(ы) становится «несбалансированным». Неуравновешенный атом называется ионом; если он получает электрон (таким образом, имея их больше, чем протонов), он становится отрицательно заряженным ионом или анионом. Если происходит обратное, и атом теряет электрон, он становится положительно заряженный ион или катион. Ионы могут соединяться с другими ионами, создавая большое разнообразие различных смесей.
Один из способов, при котором состав атомов получает или теряет электроны, — это излучение высокой энергии. Это излучение вызывает образование ионов и в результате называется ионизирующим излучением.
Электроны и электричество
Электричество — это поток электронов через проводник, обычно в виде проволоки, этот поток называется электрическим током.
Чтобы этот поток произошел, электроны должны разорвать свою атомную связь (электричество — это поток электронов, а не их поток с ядрами, с которыми они связаны). Разрыв атомной связи между электроном и его ядром требует ввода энергии, которая заставляет электрон преодолевать электромагнитную силу, сдерживающую его, и таким образом свободно течь.
Проводящий материал
Все формы материи содержат электроны, однако в некоторых материалах они более свободно связаны с их ядрами. Эти материалы (известные как проводники или металлы) требуют очень мало энергии для создания электрического тока, потому что слабо связанные электроны требуют гораздо меньше энергии для преодоления электромагнитной силы, удерживающей их на месте.
Что генерирует поток электронов?
Поток электронов можно генерировать различными способами, но основные из них следующие:
- Электрические генераторы — это устройства, использующие принцип электромагнитной индукции. Электромагнитная индукция это процесс перемещения проводника через магнитное поле с целью создания электронного потока. Требуется только относительное движение проводника и магнитного поля, что означает, что магнитное поле может двигаться, пока проводник неподвижен. Когда электроны в проводнике проходят через магнитное поле (если поле достаточно сильное, а относительная скорость проводников через поле достаточно быстрая), то связи с их ядрами будут разорваны и будет индуцирован поток. Для того чтобы вызвать высокий уровень электронного потока, необходимо большое количество энергии для создания относительной скорости между проводником и магнитами.
- Химические реакции внутри батарей также создают электродвижущую силу, заставляющую электроны течь по цепи.
- Фотоны (энергия света) также могут вызывать поток электронов, когда они сталкиваются с фотоэлектрической ячейкой расположенной в солнечной панели.
Таким образом, структура или состав атома определяет принадлежность к тому или иному химическому элементу.